小编,最近通过网络和各地药监局的互动交流中心,总结了一些医疗器械经营方面的避“坑”经验,帮助小伙伴们以备不时之需。
I. 二类医疗器械的经营备案,经营范围、经营方式要慎重选择
有质量负责人为了图省事,在选择经营范围的时候把医疗器械所有分类类目,都选上了或者选择不全,经营范围有如下几个“坑”:
① 选择经营类目过少, 未选择上经营的医疗器械
比如选择的经营范围未包含物理治疗器械类目,不能经营医用静脉曲张袜;经营范围没有医用诊查和监护器械类目,不能销售体温计;经营范围没有呼吸、麻醉和急救器械类目,不能经营医用压缩雾化器等。
解决方法:在经营引入新品类前,在国家药品监督管理局官网,查询该品类的类目分类等详细信息。
国家药监局医疗器械数据查询地址
② 选择经营类目过多,经营条件不达标
比如图省事将所有类目全部选上,在药监审查时会遇到,人员配备、仓储面积、设备设施无法达标等情况。
解决方法:提前查看新版《医疗器械经营质量管理规范》&《医疗器械经营质量管理规范现场检查指导原则》之后,了解下经营类目的选择条件,再与当地药监(或市场监督管理局)主管部门进行沟通,做到有的放矢。
③ 经营方式一味选择批零兼营
现在大多数省份要求,经营方式有零售的,必须有对外销售的门头和相关陈列要求。
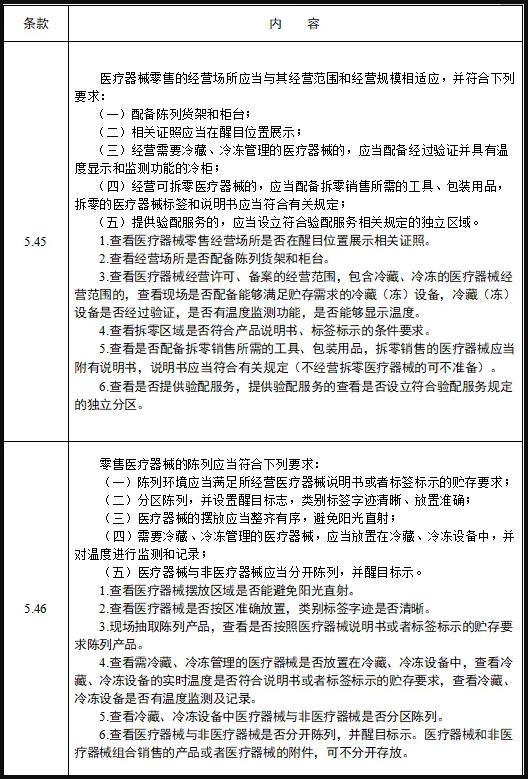
摘自《医疗器械经营质量管理规范现场检查指导原则》
II. 有些二类医疗器械可以免于备案
国家药监局关于公布《免于经营备案的第二类医疗器械产品目录》的公告(2021年第86 号)里边规定了电子血压计、水印血压表、轮椅、医用脱脂纱布等13种二类医疗器械属于免于二类经营备案的产品。但是产品首营资质审核,进货单据、检验报告还是需要有的。
III. 医疗器械标签和说明书管理规范
医疗器械的包装设计必须符合《医疗器械标签和说明书管理规范》,大多数人不注意,比如:
① 产品包装上的产品结构组成/产品描述与审批的不一致,私自修改,或者实货与产品组成/描述不一致。
解决方法:首营审核的时候,在国家药品监督管理局网站依据产品备案号或者产品注册证号查询其产品结构组成/产品描述,对照产品包装和实物进行核对。
国家药监局医疗器械数据查询地址
② 产品说明书缺少规范规定的内容
有些医疗器械生产厂家审稿不严密,包装说明书可能会缺少产品性能、安装方法、售后服务单位等内容。有些省份的主管部门要求医疗器械产品说明书上必须印有产品说明书几个字进行提示 。
解决方法:对照《医疗器械标签和说明书管理规范》进行核对。
医疗器械说明书和标签管理规定
IV. 医疗器械区的陈列
有些医疗器械产品,个别厂家会按照消毒产品进行备案申请,或者申请执行企业标准文号, 虽然产品名称一样,但是类目不一样,陈列错误容易处罚。
解决方法:熟悉各类产品的批文格式,培训到位,严格按照店内标识陈列摆放。医疗器械产品的执行标准为X械注准XXXX或者XX械备XXXXXXXX;
消毒产品要印有卫生许可证号X消卫证字XXXXXXX;
日用企标产品执行标准为Q/XXXXXXXX。
国家药监局关于印发医疗器械经营质量管理规范现场检查指导原则的通知

摘自《医疗器械经营质量管理规范现场检查指导原则》
对于医疗器械的经营管理 , 以上几个“坑”是比较容易忽略的。医疗器械经营类的相关法规主要有《医疗器械监督管理条例》、《医疗器械经营监督管理办法》、《医疗器械经营质量管理规范》, 对于医疗器械经营企业的质量管理相关人员,必须多学习多了解,烂熟于心。
相关链接:
医疗器械经营监督管理办法
素材来源于网络